
Max Planck Twente Center für Dynamik komplexer Fluide
Von kolloidalen Fluiden zu funktionalen Materialien

Das Zentrum des Max-Planck-Universität Twente Centers ist ein Forschungsnetzwerk, das sich mit der Komplexität der Strömungsmechanik befasst. Das Grundwissen in diesem interdisziplinären Thema ist für zahlreiche Bereiche relevant, wie nachhaltige Energie, medizinische Lab-on-a-Chip-Systeme oder Klima. Der Schwerpunkt der Landfester-Gruppe im Max-Planck-Twente Center liegt auf dem Verständnis der Dynamik von kolloidhaltigen Mehrphasenflüssigkeiten, die derzeit für materialwissenschaftliche Anwendungen fehlen. Wir beschäftigen uns mit verschiedenen Fragen der Selbstorganisation oder Mikrofabrikation kolloidaler Flüssigkeiten, um die Eigenschaften einzelner Kolloide mit ihrem Verhalten in Flüssigkeiten zu verknüpfen und die Eigenschaften der resultierenden Materialien maßzuschneidern.
Suprapartikel durch Trocknen von Ferrofluidtröpfchen

Superparamagnetismus existiert nur in Nanokristallen, und daher müssen sich superparamagnetische Nanopartikel zu komplexen Strukturen zusammenlagern, um superparamagnetische Materialien zu erhalten. Die meisten Techniken zur Herstellung solcher Baugruppen sind zeitlich und materiell ineffizient. Wir verwendeten eine verdampfungsgeführte Anordnung, um superparamagnetische Suprapartikel herzustellen. Durch Abstimmung der Konzentration von Ferrofluidtröpfchen und des Magnetfelds wurden superparamagnetische Suprapartikel mit unterschiedlichen Strukturen erhalten. Dieser Ansatz ist universell und kann erweitert werden, um Materialien mit höherer Komplexität zu entwerfen und andere Kolloide zu integrieren. Wir nutzten die magnetische und anisotrope Natur der resultierenden Suprapartikel, um magnetisch ansteuerbare Mikroschwimmer herzustellen.
Kontrollierte Nanopartikelproduktion durch Mikrofluidisierung

Polymer-Nanoträger werden als Transportmodule in der nächsten Generation der Wirkstofftechnologie eingesetzt. Die Leistung nanoskaliger Wirkstoffträger hängt stark von ihren physikochemischen Eigenschaften ab. Daher hängt der Erfolg neuer Nanoträger stark von unserer Fähigkeit ab, ihre Synthese in großem Maßstab präzise zu steuern. Bis vor kurzem wurden sowohl grundlegende als auch translationale Studien durch die Schwierigkeit erschwert, mit den derzeitigen Methoden monodisperse Nanoträger in großen Mengen und mit hoher Reproduzierbarkeit herzustellen. Wir haben einen vielseitigen und skalierbaren Ansatz für die Synthese von Polymer-Nanoträgern in großem Maßstab aus Wasser-in-Öl-Miniemulsionen unter Verwendung von Mikrofluidisierung entwickelt, um eine kontrollierte Emulgierung zu erreichen. Diese Methode erwies sich als effektiv bei der Herstellung von Nanoträgern mit verschiedenen Biopolymeren, einschließlich Polysacchariden, Lignin und Proteinen, mit Ausbeuten von bis zu 43 g min−1 bei reproduzierbarer Größe und Größenverteilung.
Partikel im Blutfluss
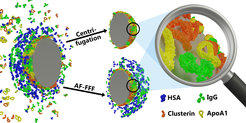
Wenn Nanoträger, die zur Arzneimittelabgabe verwendet werden, mit biologischen Flüssigkeiten in Kontakt kommen, adsorbieren Proteine an der Oberfläche der Nanoträger und bilden die Proteinkorona. Um die Nanomedizin sicher und zuverlässig zu machen, ist es erforderlich, einen besseren Einblick in die Proteinkorona zu erhalten. Wir haben die asymmetrische Feld-Fluss-Fraktionierung (AF4) als neue Separationstechnik eingeführt. Mittels AF4 konnten wir Nanopartikel inklusive nicht nur einer harten Korona mit stark gebundenen Proteinen, sondern auch der weichen Proteinkorona mit locker gebundenen Proteinen zur weiteren Charakterisierung trennen. Damit konnten wir zeigen, dass nur die harte Proteinkorona das Zellaufnahmeverhalten direkt beeinflusste.
Fluss in Pflanzen
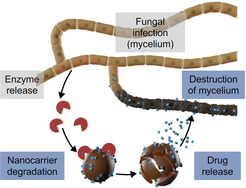
Pilzkrankheiten erfordern das Versprühen eines Fungizids, was zu Umweltschäden führt. Hier haben wir den Fluss in Pflanzenstämmen verwendet, um die erste durch Nanoträger vermittelte Wirkstoffabgabe in Pflanzen zu entwickeln. Enzymabbaubare Lignin-Nanoträger werden in die Stämme von Weinrebenpflanzen injiziert. Sie setzen selektiv ein Fungizid in den Pflanzen frei und können erstmals die weltweite Pilzkrankheit Esca heilen. Diese Strategie wird das umfangreiche Versprühen von Pestiziden in der Landwirtschaft verringern.




