
Willkommen in der Zelle!
Projekt „MaxSynBio“ stellt künstliche Zellen her
„Hier sind wir in der Hülle, die unsere Zelle umgibt“, sagt der mit Schirmmütze bekleidete Reiseleiter. Ein kleines, Raumschiff-artiges Gefährt mit einer großen Glaskuppel bewegt sich durch eine orange-blaue, biologisch wirkende Umgebung. Die erste Folge der Serie „Es war einmal das Leben“, welche 1986 produziert wurde, zeigt die Vorgänge in Zellen. Was schnell in dem 25 minütigen Animationsfilm klar wird: Die Prozesse in Zellen sind komplex! Golgi-Apparat, Mitochondrien, Lysosome und viele andere Teile arbeiten zusammen, um die Zelle am Leben zu erhalten, sie mit Energie zu versorgen oder auch Krankheiten, wie Viren, abzuwehren.
„Wir wollten solche Zellen als Beispiel nehmen und einzelne Funktionen künstlich nachbilden“, sagt Katharina Landfester, Direktorin am Max-Planck-Institut für Polymerforschung. Sie leitet ein Unterprojekt des institutsübergreifenden Projekts „MaxSynBio“. Das Ziel dieses Unterprojekts: Die Erzeugung künstlicher Miniatur-Zellen. „Nur wenn wir selbst Zellen Schritt für Schritt nachbauen, können wir verstehen, wie echte Zellen funktionieren“, so Landfester. Sie fügt hinzu: „Am Ende verstehen wir so besser, wie Leben in seinen Grundzügen funktioniert.“
Zellen aus dem Baukasten
Um künstlichen Zellen zu erzeugen, benötigen die Wissenschaftlerinnen und Wissenschaftler um Landfester grundsätzlich zwei Komponenten: Eine Schale, „Kompartiment“ genannt, welche den Inhalt schützt, sowie den eigentlichen, mikroskopisch kleinen Inhalt. Hülle und Inhalt bestimmen gemeinsam, welche Funktion die künstlich hergestellte Zelle erfüllen kann.
Ziel des Teilprojekts von „MaxSynBio“ am Max-Planck-Institut für Polymerforschung ist es, einen Baukasten gefüllt mit Teilen und Methoden zu erschaffen, mit denen sich solche künstlichen Zellen von Grund auf herstellen lassen. Auf diese Weise können Zellen, welche verschiedene Aufgaben erfüllen - wie zum Beispiel biologische Funktionen nachahmen - durch „einfaches“ Zusammensetzen der richtigen Teile zusammengebaut werden.
Mit diesem Prinzip können z. B. künstliche Zellen geschaffen werden, die spezielle Moleküle synthetisieren können. Hierfür muss der richtige Katalysator - also der richtige "Inhalt" - in das richtige synthetische Vesikel - also Kompartiment – einbaut werden. Oder wenn Zellen benötigt werden, welche gewebeähnliche Strukturen bilden können, kann dies erreicht werden, indem in die synthetischen Vesikel lichtreagierende Komponenten eingebaut werden, die sich bei Lichteinfall aneinander anlagern und so ein Geflecht aus miteinander verbundenen Vesikeln bilden.
Ein Haus im Miniaturformat
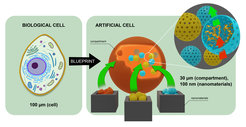
Künstliche Zellen bilden Struktur und Funktion biologischer Zellen mit synthetischen Materialien nach.
Ein wichtiger Schritt im Projekt war die Herstellung von Kompartimenten, die das Innere der Zellen umgeben und schützen: Diese Miniaturbehältnisse - die Vesikel - lassen sich nicht einfach von Hand herstellen, denn mit einer Größe von nur 20-30 Mikrometern - also Millionstel Metern - sind sie dafür viel zu klein. Es bedarf ausgeklügelter Herstellungsmethoden, mit denen diese Schalen hergestellt werden können. Und damit nicht genug: Bei der Herstellung der Schalen müssen alle Komponenten, die man im Inneren der künstlichen Zelle haben möchte, auch gleichzeitig integriert werden!
Um die Schalen herzustellen hat das Wissenschaftlerteam einen speziellen Polymertyp verwendet: ein langkettiges Molekül, ein so genanntes Blockcopolymer. Dieses kann sich in Gegenwart von Wasser mit benachbarten Blockcopolymeren vernetzen und so eine stabile Hülle erzeugen.
Die Blockcopolymere selbst werden durch chemisches Verbinden zweier „Blöcke“ hergestellt: Eine "wasservermeidenden" Polymerkette wird mit einer "wassersuchenden" Ketter verbunden. Sobald ein solches Material mit Wasser in Kontakt kommt, versuchen die wasservermeidenden Blöcke sich so zu orientieren, dass sie vor dem Wasser geschützt ist. So entsteht eine Membran mit einer im Wesentlichen "trockenen" Schicht, die von dem schützenden "wassersuchenden" Block umgeben ist, der in direktem Kontakt mit Wasser ist. Durch die Verwendung der richtigen Materialien für jeden Block und das Einstellen ihrer Länge ist es somit möglich, Polymer-Vesikel zu erzeugen, indem man diese Materialien mit Wasser in Verbindung bringt.
In ihrer Forschung sind die Wissenschaftlerinnen und Wissenschaftler noch einen Schritt weiter gegangen und haben eine Vielzahl solcher Block-Copolymere für ihren molekularen Werkzeugkasten entwickelt, um je nach Anwendung flexibel zu sein: Einige von ihnen können sich beispielsweise nur selbst zusammenfügen, wenn sie mit Licht bestrahlt werden, andere bestehen aus speziellen wassersuchenden Blöcken, die sich viel effizienter selbst zusammenfügen als andere Materialien.
Funktion folgt Form
Parallel zur Erforschung der Möglichkeiten, Vesikel mit besonderen Eigenschaften herzustellen, beschäftigt sich ein weiterer Teil des Projekts mit der Produktion der aktiven Komponenten, die sich im Inneren der Hüllen befinden. Dazu werden, wie auch bei der Herstellung der Vesikel selbst, chemische Methoden verwendet, um kleine Nanopartikel herzustellen. Diese ähneln einem Schwamm oder einem Hohlkörper und können mit Chemikalien, wie Medikamenten oder Katalysatoren, beladen werden. Diese sehr kleinen Partikel haben typischerweise einen Durchmesser von 100 Nanometern - also 100 Milliardstel Meter. Doch die winzigen Teilchen sind riesig, wenn es um ihre Funktion geht.
Im Arbeitskreis von Katharina Landfester werden Nanopartikel und Nanokapseln hergestellt, indem zunächst sehr kleine Tröpfchen erzeugt werden, die entweder in Öl oder in Wasser dispergiert sind. Reaktive Chemikalien, so genannte Monomere, die in den Tröpfchen vorhanden sind, können eine Polymerisation starten: Sie verbinden sich miteinander, wenn sie einem Auslöser - "Initiator" genannt - ausgesetzt werden. Da diese Polymerisation auf das winzige Volumen des Tröpfchens beschränkt ist, führt der Prozess zu festen Nanopartikeln oder Nanokapseln mit einer Schale, die einen flüssigen Kern umschließt. Diese können als winzige Verpackung für den Transport von Funktionsmaterialien wie Enzymen verwendet werden. Ein Vorteil dieses Ansatzes ist, dass die Beladung – also beispielsweise die Enzyme - durch das feste Nanopartikelmaterial geschützt sind und somit effizienter arbeiten können, als wenn sie frei in Lösung eingesetzt werden.
Werden spezielle Monomere verwendet, können die resultierenden Nanopartikel zudem einstellbare chemische Eigenschaften aufweisen. So kann beispielsweise dafür gesorgt werden, dass eine Reaktion nur dann ausgelöst wird, wenn der Nanopartikel mit Licht beleuchtet wird.
Energie!
In Zukunft könnten fehlerhafte Zellfunktionen mit künstlichen Zellen wiederhergestellt werden.
Doch was kann man mit einem solchen fertigen Testsystem erreicht werden? Wofür kann es eingesetzt werden? „Wir denken, dass in Zukunft solche Systeme im medizinischen Bereich eingesetzt werden können“, so Landfester.
Im menschlichen Körper spielt beispielsweise das Molekül ‚NAD‘ eine große Rolle bei der Energieversorgung der Zellen: Glukose, also Zucker, muss in Zellen in ATP umgewandelt werden. ATP ist gewissermaßen der Energielieferant der Zellen. Bei diesem Umwandlungsprozess von Glukose zu ATP fungiert NAD als eine Art Elektronenträger. Hierbei wird NAD in NADH umgewandelt – eine ähnliche, aber dennoch andere Substanz. NAD wird also „verbraucht“.
Wird neues NAD benötigt, weil beispielsweise der Körper wieder Glukose zu ATP umwandeln will, stellt der Körper das Molekül zielgerichtet an den Stellen und zu den Zeitpunkten her, wo es benötigt wird.
„Wir wollten nun einen anderen Weg gehen und NAD wieder aus NADH gewinnen – und zwar immer dann, wenn wir es wollen“, erklärt Landfester. Dafür haben die Forschenden ein komplett synthetisches System hergestellt, welches NAD aus NADH herstellen kann – NADH also „recycelt“. Der Prozess wird immer dann ausgelöst, wenn das System mit Licht bestrahlt wird und kann somit von außen gesteuert werden.














